Практикум 9. Структура и свойства аминокислот. ChemSketch. Задания
Форма отчетности по этому практикуму: протокол в формате .doc или .docx. Рекомендуется использовать формат .doc.
Проверяется (как и в прошлом блоке) файл XXXXXXX_pr9.doc (или docx) в директории term1/block2/credits.
Срок сдачи отчета: 23:59 10.11.2012. [По многочисленным просьбам, а также дабы дать время подумать над оформлением протоколов]
Внимание: в отчете запрещается использовать готовые заготовки аминокислот, которые есть в ChemSketch. Лучше структура будет немного несимметричной и косоватой. Вероятность случайного воспроизведения в точности (или намеренно попортив) заготовки из программы будет считаться равной нулю, а нарушители будут на зачете отдельно показывать свое владение ChemSketch. |
Задание №1
Пояснение к заданию: В таблице 1 приведено соответствие между студентом и тремя аминокислотами, с которыми предстоит работать в задании.
Задание:
С помощью программы ChemSketch изобразите две последовательные химические реакции, ведущие к образованию пептида XYZ, состоящего из тех аминокислот, которые Вам выданы. Исходите из предположения, что пептид синтезируется на рибосоме (в отчете в самом начале укажите, что трипептид образован при таком условии, и объясните своими словами, что оно подразумевает). Уходящие в виде молекулы воды атомы в каждой реакции выделите цветом (любым, на Ваш выбор). Подпишите аминокислоты их трехбуквенными и однобуквенными обозначениями в ChemSketch.
Сохраните получившийся файл в формате .sk2 (обычном формате ChemSketch) и в формате .pdf. В отчете приведите изображение реакций (не забудьте написать вводное предложение со ссылкой на картинку, а также подписать картинку).
Таблица 1. |
Соответствие между студентом и упорядоченных тройкой аминокислот. |
№ |
Фамилия |
Имя |
Аминокислота X |
Аминокислота Y |
Аминокислота Z |
1 |
Анисимова |
Александра |
Аланин |
Тирозин |
Лизин |
2 |
Абдрахманов |
Алибек |
Валин |
Триптофан |
Глутамат |
3 |
Андреева |
Анна |
Изолейцин |
Аргинин |
Цистеин |
4 |
Белов |
Леонид |
Метионин |
Тирозин |
Глутамат |
5 |
Галкин |
Фёдор |
Лейцин |
Треонин |
Пролин |
6 |
Гафуров |
Азамат |
Тирозин |
Лизин |
Цистеин |
7 |
Гусев |
Филипп |
Гистидин |
Тирозин |
Глутамат |
8 |
Дудина |
Дарья |
Треонин |
Цистеин |
Валин |
9 |
Ежова |
Маргарита |
Глутамат |
Изолейцин |
Серин |
10 |
Елисеев |
Алексей |
Метионин |
Лизин |
Цистеин |
11 |
Карпова |
Алла |
Глутамин |
Аргинин |
Цистеин |
12 |
Котлов |
Никита |
Валин |
Гистидин |
Тирозин |
13 |
Малеева |
Александра |
Метионин |
Глутамин |
Цистеин |
14 |
Медведев |
Дмитрий |
Валин |
Триптофан |
Цистеин |
15 |
Нуждина |
Екатерина |
Лизин |
Цистеин |
Тирозин |
16 |
Панкевич |
Евгения |
Тирозин |
Глутамат |
Валин |
17 |
Струнилин |
Илья |
Глицин |
Лизин |
Треонин |
18 |
Сутормин |
Дмитрий |
Триптофан |
Лизин |
Глутамат |
19 |
Тишина |
Софья |
Глутамин |
Гистидин |
Метионин |
20 |
Фёдорова |
Алла |
Глутамат |
Цистеин |
Валин |
21 |
Ходыкина |
Наталья |
Гистидин |
Метионин |
Триптофан |
22 |
Анфимова |
Екатерина |
Тирозин |
Глутамин |
Аргинин |
23 |
Ашниев |
Герман |
Метионин |
Тирозин |
Лизин |
24 |
Беседина |
Елизавета |
Метионин |
Лизин |
Глутамат |
25 |
Бикметов |
Дмитрий |
Фенилаланин |
Серин |
Треонин |
26 |
Босхомджиева |
Баина |
Гистидин |
Пролин |
Изолейцин |
27 |
Вакуленко |
Юлия |
Пролин |
Фенилаланин |
Валин |
28 |
Дёмин |
Олег |
Пролин |
Треонин |
Серин |
29 |
Дианов |
Дмитрий |
Метионин |
Серин |
Треонин |
30 |
Евстафьева |
Диана |
Лейцин |
Аспарагин |
Метионин |
31 |
Козлова |
Мария |
Серин |
Треонин |
Изолейцин |
32 |
Ляпунов |
Александр |
Изолейцин |
Изолейцин |
Цистеин |
33 |
Меерсон |
Марк |
Фенилаланин |
Валин |
Пролин |
34 |
Новикова |
Мария |
Лизин |
Лейцин |
Аспартат |
35 |
Носикова |
Екатерина |
Пролин |
Цистеин |
Фенилаланин |
36 |
Образцова |
Анна |
Изолейцин |
Лизин |
Аспартат |
37 |
Попов |
Ярослав |
Треонин |
Триптофан |
Аспартат |
38 |
Севастьянова |
Виктория |
Фенилаланин |
Изолейцин |
Метионин |
39 |
Травин |
Дмитрий |
Цистеин |
Триптофан |
Пролин |
40 |
Трушина |
Наталия |
Изолейцин |
Серин |
Цистеин |
41 |
Шафиков |
Радик |
Треонин |
Лейцин |
Триптофан |
42 |
Шеботинова |
Елена |
Метионин |
Треонин |
Фенилаланин |
43 |
Рябых |
Григорий |
Лизин |
Триптофан |
Валин |
44 |
Климчук |
Олеся |
Фенилаланин |
Аспартат |
Изолейцин |
Задание №2
Пояснение к заданию: При ответе на вопросы этого задания либо цитируйте вопрос, выделяя его другим стилем, например, курсивом (чтобы он явно отличался от основного текста), либо включайте его в повествовательной форме в ответ. Например:
Вопрос: Какая сегодня температура на улице?
На улице +30 градусов Цельсия.
или
Сегодня на улице температура +30 градусов Цельсия.
Иными словами, в отчете должен содержаться связный текст или последовательные ответы на перечисленные вопросы, а не просто ответы.
Задание:
Ответьте на следующие вопросы, касающиеся Вашего пептида.
- Какая аминокислота находится на N-конце пептида, а какая на C-конце?
- К каким функциональным группам (из рассмотренных на занятии или выделенных в других источниках – укажите в каких) можно отнести каждую аминокислоту Вашего трипептида?
- К какому химическому классу (альфа, бета, гамма и т.п.) относится каждая из аминокислот Вашего пептида?
Задание №3* (необязательное, повышенной сложности)
Задание: В файле ChemSketch отметьте символом * хиральные центры. Используя возможность изображения пространственной ориентации связи (кнопки «Up Stereo Bonds» и «Down Stereo Bonds» в режиме «Structure»), укажите каким стереоизомером является каждая аминокислота Вашего трипептида и подпишите обозначение типа стереоизомера (L или D) для каждой аминокислоты. Вставьте полученное изображение в отчет. Используя тот же самый символ химической связи (если для предыдущей картинки этого задания Вы выбрали закрашенный треугольник, то тут обязательно используйте его же!) нарисуйте химическую формулу Вашего трипептида с другим стереоизомером аминокислоты Y. Вставьте полученное изображение в отчет.
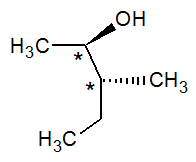
Подсказка к заданию: На рисунке 1 изображена произвольная молекула с двумя хиральными атомами углерода. Связь, отображенная символом залитого треугольника, указывает на следующее: если все связи, нарисованные обычным способом при том же атоме, разместить в плоскости, то группа, на которую она указывает (в нашем случае - OH) будет направлена на наблюдателя. Соответственно, второй тип связи указывает направление от наблюдателя.
|
Рис.1. Пример изображения пространственной конфигурации молекулы особым типом связей при хиральных (отмеченных звездочкой) атомах углерода. Группа OH при втором атоме углерода направлена на наблюдателя, а группа CH3 при третьем атоме углерода – от наблюдателя. |


 2023
2023 2022
2022 2021
2021 2020
2020 2019
2019 2018
2018
 2017
2017 2016
2016