Название структуры: кристаллическая структура белка BIOH AT 1.7 A
В документе представлены следующие цепи макромолекул:
Идентификатор цепи |
Число остатков |
Название молекулы |
Комментарии |
A |
258 |
BIOH proteine |
Белок BIOH,
|
В документе представлены следующие низкомолекулярные вещества:
ID |
Название |
Формула |
Число копий |
Комментарии |
MSE |
SELENOMETHIONINE
|
C5H11NO2SE |
5 (в структуре их 6,
|
Модифицированная аминокислота,
|
3OH |
3-HYDROXY-PROPANOIC ACID
|
C3H6O3 |
1 |
|
EDO |
1,2-ETHANEDIOL
|
C2H6O2 |
2 |
|
HOH |
Water (вода) |
H2O |
258 |
Не вынесена в поля
|
Рассмотрим подробнее документ 1m33.pdb.
HEADER STRUCTURAL GENOMICS, UNKNOWN FUNCTION 26-JUN-02 1M33
TITLE CRYSTAL STRUCTURE OF BIOH AT 1.7 A
Заголовок структуры: белок с неизвестной функцией.
Название структуры: кристаллическая структура белка BIOH AT 1.7 A
COMPND MOL_ID: 1;
COMPND 2 MOLECULE: BIOH PROTEIN;
COMPND 3 CHAIN: A;
COMPND 4 ENGINEERED: YES
В поле «COMPND» говорится о том, что белок состоит из одной полипептидной цепи, которую авторы договорились называть «цепь А». Такой белок ученые умеют получать в ходе генноинженерного эксперимента.
Из описания гена BioH в файле ecoli_K12_U00096.embl с полностью секвенированным геномом бактерии E. Coli можно почерпнуть информацию и о белке: Ген кодирует один белок, содержащий одну аминокислотную последовательность (найдена в этом же файле). Данные о белке, взятые из разных источников совпадают (за исключением функции белка: в ecoli_K12_U00096.embl есть информация о его функции, а в pdb-файле она отсутствует) и дополняют друг друга.
SEQRES 1 A 258 MSE ASN ASN ILE TRP TRP GLN THR LYS GLY GLN GLY ASN
SEQRES 2 A 258 VAL HIS LEU VAL LEU LEU HIS GLY TRP GLY LEU ASN ALA
SEQRES 3 A 258 GLU VAL TRP ARG CYS ILE ASP GLU GLU LEU SER SER HIS
SEQRES 4 A 258 PHE THR LEU HIS LEU VAL ASP LEU PRO GLY PHE GLY ARG
SEQRES 5 A 258 SER ARG GLY PHE GLY ALA LEU SER LEU ALA ASP MSE ALA
SEQRES 6 A 258 GLU ALA VAL LEU GLN GLN ALA PRO ASP LYS ALA ILE TRP
SEQRES 7 A 258 LEU GLY TRP SER LEU GLY GLY LEU VAL ALA SER GLN ILE
SEQRES 8 A 258 ALA LEU THR HIS PRO GLU ARG VAL ARG ALA LEU VAL THR
SEQRES 9 A 258 VAL ALA SER SER PRO CYS PHE SER ALA ARG ASP GLU TRP
SEQRES 10 A 258 PRO GLY ILE LYS PRO ASP VAL LEU ALA GLY PHE GLN GLN
SEQRES 11 A 258 GLN LEU SER ASP ASP GLN GLN ARG THR VAL GLU ARG PHE
SEQRES 12 A 258 LEU ALA LEU GLN THR MSE GLY THR GLU THR ALA ARG GLN
SEQRES 13 A 258 ASP ALA ARG ALA LEU LYS LYS THR VAL LEU ALA LEU PRO
SEQRES 14 A 258 MSE PRO GLU VAL ASP VAL LEU ASN GLY GLY LEU GLU ILE
SEQRES 15 A 258 LEU LYS THR VAL ASP LEU ARG GLN PRO LEU GLN ASN VAL
SEQRES 16 A 258 SER MSE PRO PHE LEU ARG LEU TYR GLY TYR LEU ASP GLY
SEQRES 17 A 258 LEU VAL PRO ARG LYS VAL VAL PRO MSE LEU ASP LYS LEU
SEQRES 18 A 258 TRP PRO HIS SER GLU SER TYR ILE PHE ALA LYS ALA ALA
SEQRES 19 A 258 HIS ALA PRO PHE ILE SER HIS PRO ALA GLU PHE CYS HIS
SEQRES 20 A 258 LEU LEU VAL ALA LEU LYS GLN ARG VAL GLY SER
Количество аминокислот и их последовательность совпадают по данным в ecoli_K12_U00096.embl и в 1М33.pdb: белок содержит 258 остатков, что говорит о том, что белок в организме бактерии не теряет часть последовательности, а сохраняется целиком. Однако не совпадают некоторые трёхбуквенные обозначения амнокислот: в 1М33.pdb аминокислота метионин, вместо Met, обозначается Mse.
HET MSE A 64 8
HET MSE A 149 12
HET MSE A 170 12
HET MSE A 197 11
HET MSE A 217 12
HET 3OH A 300 12
HET EDO 301 4
HET EDO 302 8
HETNAM MSE SELENOMETHIONINE
HETNAM 3OH 3-HYDROXY-PROPANOIC ACID
HETNAM EDO 1,2-ETHANEDIOL
HETSYN EDO ETHYLENE GLYCOL
FORMUL 1 MSE 5(C5 H11 N O2 SE)
FORMUL 2 3OH C3 H6 O3
FORMUL 3 EDO 2(C2 H6 O2)
FORMUL 5 HOH *238(H2 O)
К «необычным» для белковой структуры авторы отнесли производную аминокислоты метионина – селенометионин (Mse), который 6 раз встречается в белке (нет немодифицированного метионина в белке). Авторы почему-то не указали в полях HET селенометионин, начинающий аминокислотную последовательность. В описание структуры также попали 2 молекулы 1,2-этандиола (EDO), 238 молекул воды и одна молекула 3-гидроксипропановой кислоты (3OH). В полях FORMUL даны формулы этих соезинений.
Посмотрим на пространственное строение остова белка:
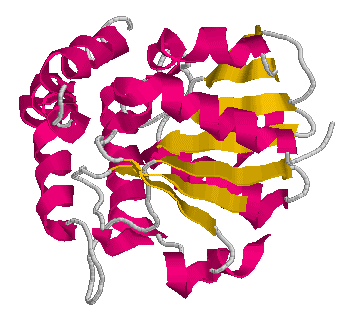
|
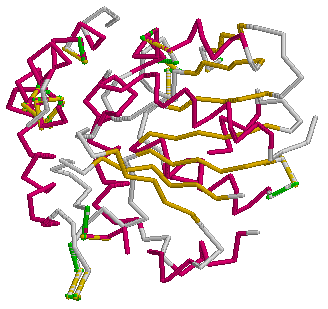
|
| На рисунках розовым цветом обозначены участки альфа-спиралей, жёлтым - бета-тяжей, серым - участки, не имеющие регулярной вторичной структуры |
Белок имеет альфа-спиральные и бета-складчатые участки, чередующиеся друг с другом, примерно в равных количествах.